
Editorial
Les maladies génétiques prédisposant aux cancers sont nombreuses et variées.…

Les maladies génétiques prédisposant aux cancers sont nombreuses et variées.…

En 2017, on retiendra en oncodermatologie essentiellement l’arrivée de traitements…
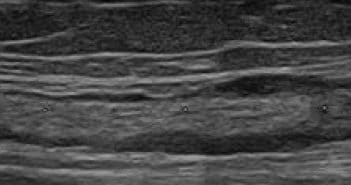
La plupart des cancers cutanés ont un mode de dissémination lymphophile exclusif ou accessoire. La recherche précoce d’un envahissement ganglionnaire est un des enjeux de leur prise en charge et l’échographie y occupe une place de choix. Mais sa sémiologie est mal connue des prescripteurs, source de confusions fréquentes.
Nous verrons l’architecture ganglionnaire physiologique, les variations anatomiques et les signes d’envahissement en fonction des types tumoraux.
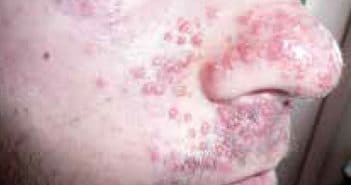
Les maladies granulomateuses sont fréquentes en dermatologie et leurs étiologies multiples (infectieuses, inflammatoires, auto-immunes…). Les causes de granulomes sont notamment les plus nombreuses lorsque les lésions sont localisées au visage : pathologies localisées (infections d’inoculation, granulome silicotique) ou systémiques (sarcoïdose), de causes identifiables (mycobactériose) ou idiopathiques (lupus miliaire disséminé). Certaines maladies ont une présentation granulomateuse systématique alors que d’autres dermatoses peuvent se présenter de façon occasionnelle par des granulomes (lymphomes cutanés primitifs ou secondaires) ou au cours de leur évolution (rosacée granulomateuse).
Le caractère granulomateux des lésions n’est pas toujours cliniquement évident, et même si certains aspects sont évocateurs, le diagnostic requiert fréquemment une confrontation anatomoclinique.
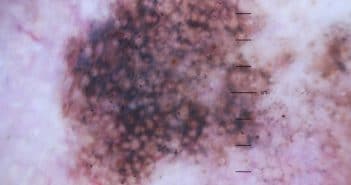
Une véritable révolution thérapeutique a eu lieu dans le mélanome métastatique depuis 2011 grâce aux immunothérapies et aux thérapies ciblées. À ce jour, le traitement de 1re intention des mélanomes mutés BRAF est l’association d’inhibiteurs de BRAF et de MEK, et celui des mélanomes BRAF sauvage est l’anti-PD-1.
L’intérêt de traiter précocement les patients mutés par immunothérapie reste à évaluer. L’apparition de résistances secondaires en cours de thérapies ciblées est une vraie problématique et pourrait être limitée grâce à un traitement intermittent ou séquentiel. Après échappement thérapeutique, l’ajout d’une 3e molécule choisie selon les mécanismes de résistance apparus est en cours d’étude. Les options thérapeutiques pour les patients BRAF sauvages restent limitées avec de l’espoir dans les associations de thérapies ciblées et d’immunothérapies. La gestion de la tolérance de traitements utilisés sur des durées prolongées est essentielle.
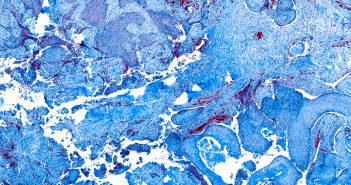
Une actualisation des recommandations EORTC (European Organisation for Research and…
Les toxicités des immunothérapies du mélanome (anticorps anti-CTLA4 et anticorps…
Prise en charge des mélanomes stades I à III Le…
Les immunothérapies anticancéreuses anti-CTLA-4, puis anti-PD-1 et anti-PD-L1, ont modifié le pronostic des mélanomes. Leur mécanisme d’action explique probablement en grande partie leurs effets indésirables, notamment cutanés, de nature volontiers “auto-immune”. Bien que rarement sévères, ces derniers peuvent être majorés en fréquence et en sévérité dans le cas d’association de plusieurs molécules d’immunothérapie, qui est une voie de recherche actuelle.
Les thérapies ciblées anticancéreuses ont une toxicité cutanée fréquente et spécifique, différente de celle des chimiothérapies et immunothérapies (tableau I). De plus en plus, un avis dermatologique est sollicité pour la prise en charge des patients traités par ces molécules.
Il est donc important pour le dermatologue de connaître, de savoir évaluer ces effets secondaires cutanés et d’avoir des notions sur leur prise en charge, notamment les plus classiques comme les éruptions acnéiformes sous anti-EGFR, le syndrome main-pied sous anti-BRAF ou les paronychies sous anti-EGFR ou inhibiteurs de mTOR. Il s’agit véritablement de soins de support dermatologiques qui doivent permettre, dans la mesure du possible, de poursuivre les traitements dans l’intérêt du patient.
