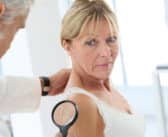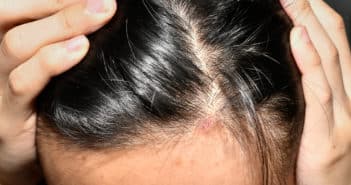
Cuir chevelu squameux : les pièges et la prise en charge
Les laboratoires Vichy ont organisé au cours des dernières JDP un symposium consacré aux maladies squameuses du cuir chevelu, essentiellement la dermatite séborrhéique (et les états pelliculaires) et le psoriasis.
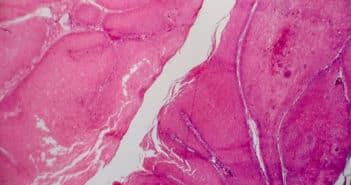
Condylomes : prise en charge des cas difficiles
Les condylomes sont principalement dus aux papillomavirus humains non oncogènes et sont une infection sexuellement transmissible. La prise en charge de ces lésions est peu codifiée et souvent complexe pour le praticien. Certaines situations cliniques comme les condylomes récidivants et/ou multiples, mais aussi leur présence chez des populations spécifiques (immunodéprimés ou chez les femmes enceintes), nécessitent un ajustement de ses pratiques habituelles. Les principaux traitements utilisés sont les traitements ablatifs, immunomodulateurs, chimiques (appliqués par le patient ou le médecin) et sont à adapter aux patients. Une prise en charge multidisciplinaire est parfois nécessaire.
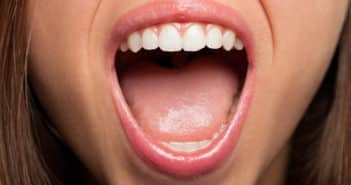
Éditorial – Dossier : Pathologies buccales de l’adulte
La pathologie de la muqueuse buccale nous invite à toutes les surprises. Ce territoire aux frontières floues entre peau et muqueuse devient un lieu de prédilection pour assurer un diagnostic. Les dermatologues ont entrepris de s’en occuper de façon particulière et d’examiner systématiquement la muqueuse buccale de leurs patients.
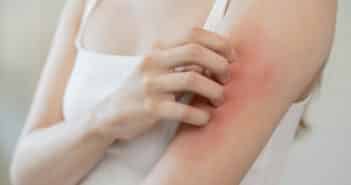
Questions flash – Allergologie et environnement
Les changements de climats et des températures modifient le risque de maladies vectorielles et de maladies liées à l’eau. Enfin, le réchauffement du climat avec la fonte des glaciers expose à la réémergence de microbes préhistoriques appelés les “super bugs” avec une résistance aux anti-infectieux partiellement inconnue.
Dans ce flash, nous rappellerons quelques cas de maladies vectorielles importantes à connaître pour le dermatologue, quelques dermatoses liées à l’eau et expliquerons le concept de “super bugs”.

Perturbateurs endocriniens et toxicité environnementale des cosmétiques
De multiples critiques sont faites sur les ingrédients des cosmétiques. En ce qui concerne le risque sur la santé humaine, on reproche à certains composants leurs risques photo-allergisants de contact, d’être des perturbateurs endocriniens (PE), d’avoir un pouvoir oncogène et de ne pas pouvoir être détruits par l’organisme dans lequel ils auraient pénétré comme pour les nanoparticules ou les PFAs [1]. On leur reproche aussi un impact environnemental négatif par leurs composants perturbateurs endocriniens, leur impact sur les coraux, la faune et la flore marines, le recours à des composants dérivés de la pétrochimie et l’utilisation de plastique pour leurs emballages ou la consommation d’eau qu’ils induisent.
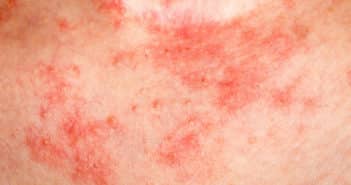
Actualités dans l’urticaire
L’urticaire chronique (UC) est une maladie fréquente. Son incidence est d’environ 1 %, avec une nette prédominance féminine chez l’adulte [1].

Actualités sur les nouveaux allergènes de contact
Les années 2022-2023 ont été marquées par une actualité riche en dermato-allergologie, avec notamment une réactualisation de la batterie standard européenne des patch-tests. Des allergènes des cosmétiques, des tatouages ou professionnels ont également fait l’objet d’intéressantes mises au point.
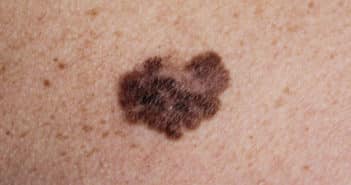
Actualités sur la prise en charge du mélanome
La prise en charge du mélanome s’est considérablement modifiée depuis ces 12 dernières années.
L’un des progrès majeurs découle de la découverte d’une mutation somatique du gène codant pour la sérine-thréonine kinase BRAF dans environ 50 % des mélanomes. Cette mutation active de façon constitutive la voie des MAP- kinases. Elle a été à l’origine du développement des thérapies ciblées dirigées contre cette enzyme BRAF mutée, puis dans un deuxième temps de l’augmentation de la puissance de ce traitement ciblé en combinant les anti BRAF avec des anti-MEK. À ce jour, la combinaison anti-BRAF + anti-MEK nous permet d’obtenir 70 % de réponses objectives chez les patients atteints de mélanome métastatique. En revanche, ces traitements, bien que très efficaces en termes de réponse clinique, ont une durée d’efficacité limitée dans le temps. La survie sans progression est d’environ 15-18 mois, et les résistances sont difficiles à combattre lorsqu’elles surviennent.
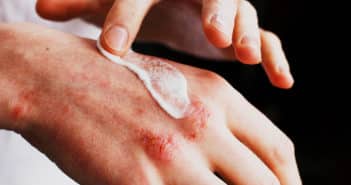
Quoi de neuf dans la physiopathologie des eczémas ?
De nouveaux traitements sont enfin disponibles pour la prise en charge de la dermatite atopique (DA) et l’eczéma des mains (ECM). Ces approches innovantes nous font progresser dans la connaissance de la physiopathologie complexe des eczémas.
Questions flash – Cancérologie cutanée
Les kératoses actiniques (KA) ont une présentation clinique multiforme mais une rugosité constante et beaucoup se palpent plus qu’elles ne se voient. Elles surviennent en zone photo-exposée et leur incidence double tous les 10 ans de façon proportionnelle au vieillissement de la population [1]. Leur risque de progression vers un carcinome épidermoïde invasif pour des lésions individuelles varie de 0,025 % à 16 % par an, avec un risque de 10 % à 10 ans. Les KA sont retrouvées comme précurseur de 60 % des carcinomes épidermoïdes cutanés (CEC) [2]. Induites par la dose totale d’UV cumulés elles sont multiples, visibles et invisibles, en champs de cancérisation sur ces zones photo-exposées que sont le front et le crâne glabre. Il apparaît logique de traiter ces zones afin de minimiser le risque de progression vers un CEC.