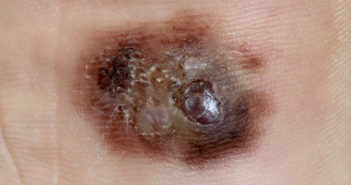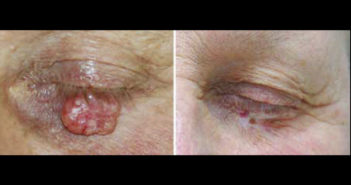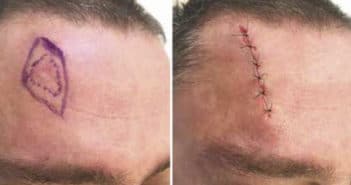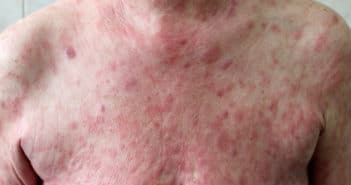
Face au mycosis fongoïde et au syndrome de Sézary : quelles stratégies thérapeutiques aujourd’hui ?
L’arsenal thérapeutique dans les lymphomes cutanés T est très large. Le choix du traitement dépend du type histologique, du stade et du terrain. Aux stades précoces, les traitements cutanés (dermocorticoïdes, chimiothérapies locales, photothérapie dynamique et photothérapie) sont utilisés en première intention. Aux stades avancés, les traitements immunomodulateurs (méthotrexate, interféron alpha et rexinoïde) sont utilisés seuls ou en association aux traitements cutanés et leur indication est validée en RCP, en lien avec un centre de référence du GFELC.
La plupart des traitements sont suspensifs. L’émergence récente de nouvelles thérapeutiques telles que le brentuximab vedotin, le mogamulizumab ou l’anti-KIR3DL2 suscite beaucoup d’espoir.