Intelligence artificielle en oncodermatologie
L’intelligence artificielle (IA), ou plutôt les différents algorithmes qui constituent cette branche en pleine évolution des mathématiques, est d’autant plus sujette à la création de fantasmes, positifs ou négatifs, qu’il s’agit d’une discipline complexe nécessitant des compétences en mathématique de niveau supérieur pour en comprendre les mécanismes intimes et donc partagées par une partie très limitée de la population médicale. Toutefois, il n’est pas nécessaire d’être un spécialiste de l’optique pour analyser une dermatoscopie, même si le parcours de la lumière issue de la source lumineuse vers sa cible puis de la cible vers le capteur est tout sauf trivial dans sa compréhension fine de la physique de l’optique.
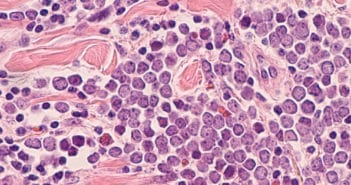
Le carcinome à cellules de Merkel et autres cancers rares : ce qu’il faut savoir
Le carcinome à cellules de Merkel est rare. Il atteint presque exclusivement les patients caucasiens. Son incidence est en augmentation rapide depuis plusieurs années dans tous les pays développés. En France, l’incidence standardisée est actuellement estimée à 0,4 pour 100 000 personnes/an.

Bases fondamentales de l’immunothérapie
Le concept d’immunosurveillance est né en 1909, quand Paul Ehrlich émet l’hypothèse que le système immunitaire de l’hôte peut prévenir le développement de tumeurs. Cette hypothèse a ensuite été longtemps abandonnée. En 1953, Gross et Foley montrent l’efficacité contre les sarcomes d’une vaccination avec des extraits de tumeur chez la souris. En 1970, Burnet formule l’hypothèse que des néoantigènes tumoraux induisent une réaction immunitaire.

Pathologie vulvaire pédiatrique : du normal au pathologique
Les vulvo-vaginites sont le plus souvent non spécifiques. Il n’y a pas (ou exceptionnellement) de candidose chez la petite fille. Le lichen scléreux nécessite un traitement fort, prolongé et une surveillance à vie. Les condylomes du nourrisson et du jeune enfant ne sont le plus souvent pas des IST. Penser à l’ulcération aiguë non vénérienne de Lipschutz chez la jeune fille. Garder en mémoire les causes plus rares et la possibilité d’un abus sexuel.

Toxicités cutanées et systémiques des immunothérapies
L’immunothérapie a révolutionné la prise en charge thérapeutique en cancérologie avec des taux de réponse thérapeutique inégalés et parfois extrêmement durables dans le mélanome métastatique et de nombreux cancers. Les molécules utilisées à ce jour en dermatologie sont les anti-PD-1 (nivolumab, pembrolizumab), les anti-CTLA-4 (ipilimumab) et les anti-PDL-1 (avelumab). Celles-ci entraînent des effets secondaires immunomédiés chez plus de 60 % des patients traités ; la peau étant l’organe le plus concerné. Le dermatologue est au cœur de la prise en charge de ces complications en tant que prescripteur des immunothérapies dans les tumeurs cutanées, mais aussi en tant que spécialiste d’un organe particulièrement affecté par ces traitements.
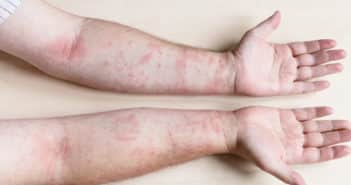
Eczémas de contact : quoi de neuf ?
De nombreux nouveaux allergènes, ou de nouvelles applications d’allergènes déjà bien connus, ont été signalés en 2021-2022. Dans cette revue, nous abordons quelques allergènes cosmétiques remarquables et/ou émergents, y compris les fragrances, les conservateurs, les allergènes végétaux, les nouveaux agents dépigmentants, et certains filtres solaires problématiques. De plus, nous faisons le point sur les nouveaux allergènes “manucure”, et détaillons de plus près les allergènes principaux dans les gants et les chaussures. Nous donnons un aperçu de quelques métaux allergisants, et mentionnerons des exemples d’allergènes importants dans les dispositifs médicaux, tels que les pansements adhésifs, les antiseptiques et les désinfectants.
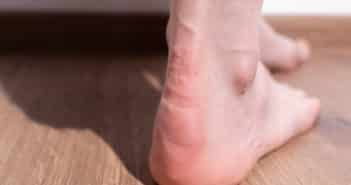
Dermatites de contact des pieds
L’environnement chaud, macéré et humide au sein d’une chaussure, combiné à l’exposition à divers allergènes potentiels (caoutchoucs, colles, colorants, agents tannants, sels de chrome, biocides, allergènes des plastiques, etc.) créent un environnement idéal pour le développement d’une dermatite allergique de contact (DAC). Sans oublier les allergènes potentiels liés aux traitements appliqués (excipients des topiques, corticoïdes, antiseptiques, antifongiques, etc.).
La DAC aux chaussures atteint la plupart du temps la surface dorsale des orteils (surtout l’hallux) ou le dos des pieds dans son entièreté.
L’atteinte plantaire est plus rare mais peut exister. En général, elle respecte la voûte plantaire. Une éruption vésiculeuse secondaire (située en particulier aux mains) peut s’observer.
La réalisation de tests épicutanés reste l’examen de choix du diagnostic de la DAC. En effet, le traitement principal réside en la découverte et l’éviction de l’(des) allergène(s) responsable(s).
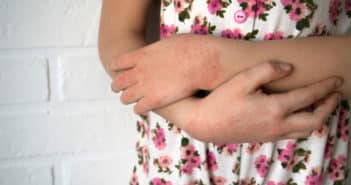
Eczémas de contact chez l’enfant
L’eczéma de contact chez l’enfant représenterait jusqu’à 20 % des dermatites pédiatriques et concerne environ un tiers des enfants avec une dermatite atopique. Ses présentations cliniques sont parfois déroutantes et les allergènes chez l’enfant sont souvent masqués et en perpétuelle évolution, dépendante des modes. S’il n’existe pas de batterie standard enfants consensuelle, on s’accorde cependant pour tester de plus en plus facilement les eczémas atopiques ou non, résistant à un traitement bien conduit, les eczémas palmoplantaires, aéroportés, de localisation inhabituelle avec des batteries de tests proches des adultes, en n’oubliant jamais de tester les produits personnels de l’enfant.

Eczémas de contact aux gants
L’allergie aux gants de protection est fréquente, notamment en milieu professionnel. Elle doit être systématiquement recherchée devant tout eczéma des mains et des poignets.
Les matériaux de gants les plus souvent incriminés sont le caoutchouc, les plastiques et le cuir. Il existe deux mécanismes différents pour l’allergie aux gants en caoutchouc. L’allergie est soit retardée, se manifestant par un eczéma de contact. Les principales causes sont les accélérateurs de vulcanisation du caoutchouc (thiurames-dithiocarbamates, guanidines, benzothiazoles et thiourées). Soit il s’agit d’une allergie immédiate médiée par les IgE, les causes étant les protéines de latex. Les gants en plastique (principalement le polychlorure de vinyle) peuvent également provoquer des eczémas de contact allergiques, l’obtention de la composition est très difficile. L’allergène des gants en cuir est le chrome.
La prévention des récidives repose sur l’éviction du contact avec les allergènes.
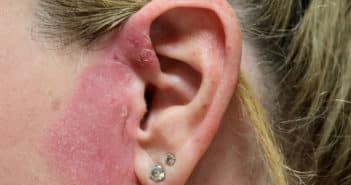
Éditorial – Dossier : Eczémas de contact
La dermatite allergique de contact (ou eczéma allergique de contact) est consécutive à l’application par voie directe ou par voie aéroportée d’une substance exogène, se comportant comme un haptène (qui se transforme en allergène complet dans l’épiderme après couplage avec une protéine) et déclenchant une réaction d’hypersensibilité à médiation cellulaire retardée (type IV). Classiquement, la dermatite allergique de contact survient après 7 à 10 jours lors du premier contact avec l’allergène (phase d’induction) et après 24 à 72 heures lors d’un contact ultérieur (phase de révélation). Il est essentiel de rappeler que la dermatite allergique de contact ne survient pas nécessairement lors du premier contact. Cette réaction allergique peut survenir après plusieurs mois ou, plus rarement, plusieurs années de tolérance. “On ne naît pas allergique, on le devient”.